![澳门威斯人游戏平台[亚洲]全站最新版V11.37.7](/wp-content/themes/2023/images/banner/technical-resources.jpg?v=18)
细胞毒性T细胞是癌症患者治疗过程中效力最高的免疫细胞群。1992年,重组IL-2(一种T细胞活化细胞因子)获得批准,以及T细胞检查点抑制剂(如PD-1拮抗抗体帕博利珠单抗和纳武利尤单抗)的临床影响,获得了T细胞在癌症治疗中重要性的早期临床证据。更直接的证据来自自体肿瘤浸润T细胞(TILs)的治疗方法,该疗法与清淋治疗和IL-2相结合,在黑色素瘤和卵巢癌患者中产生了强烈的反应。当自体T细胞被改造为表达重组嵌合抗原受体(CAR)时,只要它们能够对细胞表面抗原进行主要组织相容性复合体(MHC)非依赖性识别,就可以在液体肿瘤中观察到高完全缓解率和持久反应,已有几种靶向CD3或BCMA的CAR-T疗法获得批准。尽管细胞疗法在非实体瘤中获得临床成功,但该治疗可能具有显著毒性,且在实体瘤中的活性有限。
T细胞衔接器(T cell engager, TCE)是细胞因子、检查点抑制剂和T细胞疗法的替代疗法,它们通常基于抗体或抗体片段,能够将体内任何T细胞与表达选定表面标志物的细胞连接起来。TCE可以精确控制剂量和摄入时间,有助于最大限度地减少副作用,并且生产过程比细胞疗法要简单得多。靶向CD19、CD20、BCMA的TCE在复发/难治性(r/r)急性淋巴细胞白血病(ALL)、非霍奇金淋巴瘤(NHL)、多发性骨髓瘤(MM)已经观察到令人信服的完全缓解率。
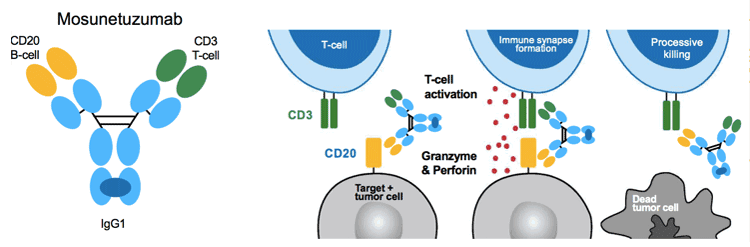
TCE一个臂靶向肿瘤相关细胞表面抗原(TAA),另一个臂靶向TCR-CD3复合物中CD3ε亚基,结合癌症细胞和T细胞。这种结合促进T细胞和癌细胞之间免疫突触的形成,T细胞可以通过突触将穿孔素和颗粒酶注入到附着的癌细胞中。突触的形成引起TCR交联和T细胞活化,引发促炎细胞因子的释放,诱导T细胞增殖。从理论上讲,每种细胞毒性T细胞表型都可以通过这种方式结合并参与连续癌细胞裂解,包括CD8+T细胞,CD4+T细胞,γ/δT细胞和NKT细胞。通过识别细胞表面抗原,TCE使得T细胞的活化摆脱了MHC分子、抗原肽加工和呈递以及TCR特异性的限制。

IgG-like TCE
Mosunetuzumab采用knobs-into-holes技术进行重链配对,采用体外退火技术进行重轻链配对,已被批准用于治疗R/R滤泡性淋巴瘤(FL)。
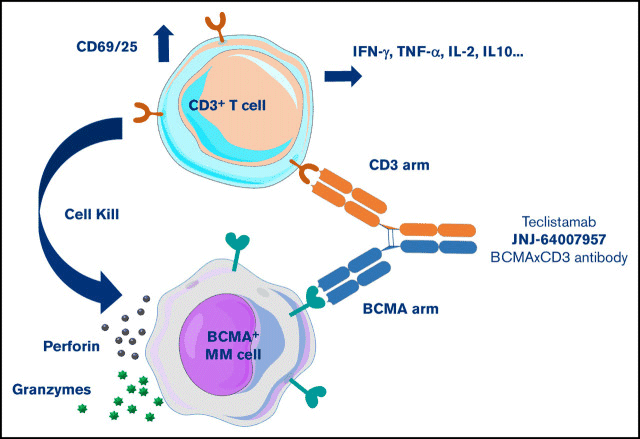
Teclistamab是一种基于Genmab公司开发DuoBody®平台的TCE,靶向BCMA/CD3,已上市用于治疗r/r多发性骨髓瘤(MM)。
DuoBody®平台利用限制性Fab臂交换技术(controlled Fab-arm exchange, cFAE),在两个IgG抗体的CH3区域分别引入K409R和F405L突变,利用哺乳动物细胞表达系统进行单独的重组表达与纯化,随后将两种抗体在定制条件下利用cFAE重新组合,即可高效组装获得具有正常IgG结构的双特异性抗体。Teclistamab抗体骨架为IgG4亚型,需要对其进行PAA突变(S228P L234A/L235A)除去IgG4的天然FAE过程和Fc的相关响应功能(ADCC,CDC)。
Epcoritamab也基于DuoBody®平台,最近被批准用于治疗R/R弥漫性大B细胞淋巴瘤(DLBCL)。
ERY974是一种靶向Glypican-3(GPC3)的TCE,用于治疗实体瘤,目前处于临床前开发阶段。它的构建是通过在CH3结构域引入静电转向突变来驱动重链的异源二聚化,同时利用共同轻链来避免轻链的错配(ART-Ig)。
REGN1979为靶向CD20/CD3的TCE,该TCE使用共同轻链,并在重链CH3区域中引入突变,形成IgG1/IgG2/IgG4与IgG3的局部同型嵌合体,利用蛋白质A的选择性纯化获得双特异性抗体。REGN1979现正在适应症恶性淋巴瘤(B-NHL)的临床试验中。
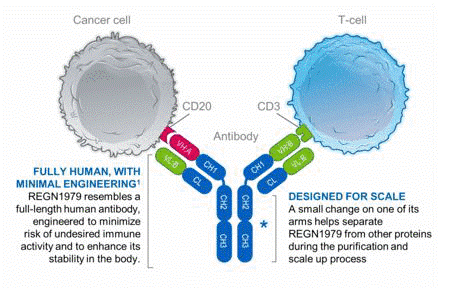
这种TCE结构有望成为一种新平台。基于该平台,还有一些用于治疗实体瘤的TCE,包括REGN4018——靶向MUC16/CD3,用于治疗卵巢癌(OC)和REGN4336——靶向PSMA/CD3,用于治疗转移性去势抵抗性前列腺癌(mCRPC),正在临床试验中。
基于抗体片段的TCE
虽然Fc-like TCE具有天然IgG的特性,有利于抗体药物的制备和PK/ADA特性,但或出于独特的医疗目的,或由于生产工艺技术或商业限制,基于抗体片段的TCE也逐渐走入视线。
基于抗体片段的TCE通常是——
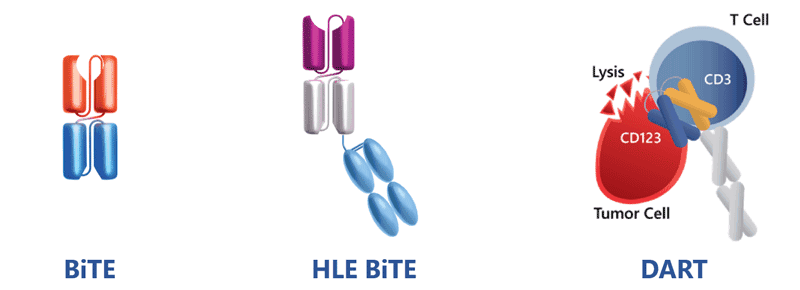
这类TCE的代表是Amgen公司基于BiTE®平台,靶向CD19/CD3的Blinatumomab,已被批准用于治疗成人急性淋巴细胞白血病(BCP-ALL)及后续更多的适应症。
为了延长半衰期,减少给药频率,Amgen在BiTE®上融合Fc结构域,产生了一系列HLE BiTE分子(分子量约为106 kD)。AMG757是一种靶向DLL3的HLE BiTEs,目前正在研究用于复发性小细胞肺癌(SCLC)治疗。
以类似的方式,MacroGenics开创了DART平台并以此平台设计了治疗性分子,这些分子将两个独立的fab以异源二聚体结构结合在一起,可根据半衰期长短进行调整,具有或不具有Fc结构域。MGD024是一种用于治疗r/r CD123(+)血液系统恶性肿瘤患者的靶向CD123/CD3的Dart TCE,目前已进入临床研究。
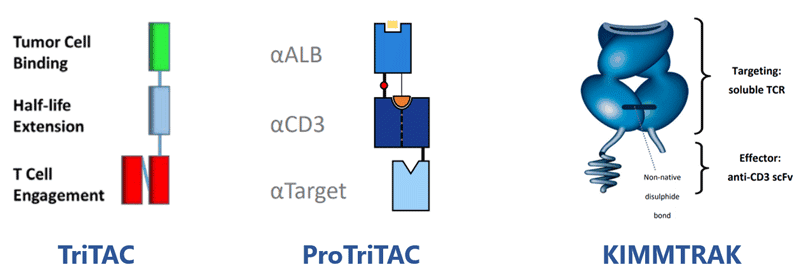
Harpoon公司开发了针对实体瘤和血液系统恶性肿瘤T细胞激活性多功能抗体,抗体基于其创建的TriTAC、ProTriTAC(前药)和TriTAC-XR三个三特异抗体平台,这些TCE平台引入了单域抗体,并通过结合白蛋白来延长半衰期。
TriTAC仅含有一条肽链,包含三个结构域,分别结合CD3,人血清白蛋白和TAA。其中结合CD3表位的抗体为单链抗体(scFv),结合人血清白蛋白和TAA的抗体为纳米抗体。
此外,Immunocore公司开发的第一种也是唯一一种被批准用于实体瘤(黏膜黑色素瘤,mUM)治疗的TCE——Tebentafusp-tebn(KIMMTRAK),由TCRm和靶向CD3的scFv组成。
其他类型的TCE
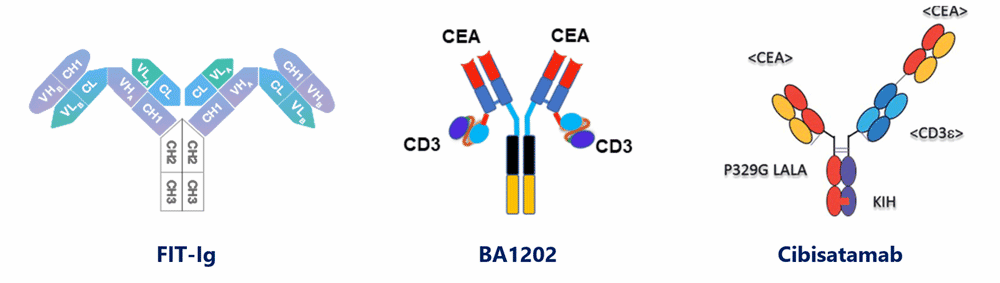
EMB-07是利用EpimAb的FIT-Ig平台设计的,靶向ROR1/CD3的TCE,用于实体瘤的治疗,目前正在进行临床评估。
Appended-IgG在常规IgG上附加scFv、Fab或纳米抗体。它们的半衰期与亲代IgG相当。然而,非自然结构可能会增加聚集性、不稳定性和ADA风险。FIT-Ig平台在不引入突变或连接子(linker)的情况下产生双特异性抗体,有利于其制备和稳定性。
EMB-06是另一种基于FIT-Ig平台的靶向BCMA的TCE,目前也在临床评估中。
BA1202为Boan Biotech靶向CEA/CD3的对称三价单链抗体,其具有类似蝴蝶形的抗体结构:Fab端与CEA双价结合,而轻链C端连接的二价单链抗体与CD3单价结合(可能是由于空间构象的改变或亲和力降低),目前已进入临床试验阶段。
Cibisatamab是一种靶向CEA/CD3的TCE,通过将第二个与CEA结合的Fab区添加到对称KIH结构来实现与疾病靶点的“低亲和力(affinity)高亲合力(avidity)”结合,试图通过减少脱靶毒性来实现疗效和安全性的平衡。目前该TCE正在临床试验中。
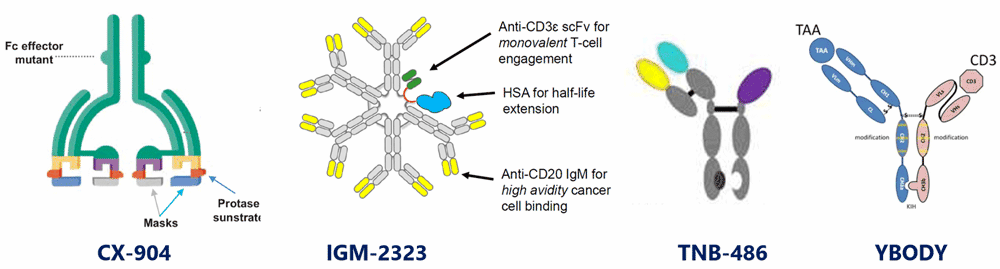
CX-904是由Cytomx公司为精准靶向设计的前体药物,在肿瘤微环境中通过特异性蛋白水解条件被激活,靶向EGFR/CD3,目前正在临床试验中。
Imvotamab是靶向CD20和CD3的IgM同种型TCE。Imvotamab拥有10个CD20结合域,比IgG同种型的抗体有更高的亲合力,从而能够克服靶点减少引起的耐药,并实现比目前已批准的抗体疗法更好的疗效。该公司更多的IgM TCE药物包括IgM-2644(CD38/CD3)和IgM-2537(CD123/CD3)。
TNB-486是一种由Tenobio公司开发靶向CD19的不对称TCE。它的形式介于IgG-like TCE和基于抗体片段TCE之间。它由一半结合CD3的IgG和一半结合CD19的重链抗体(HcAb)组成,目前正针对r/r B淋巴瘤进行临床评估。
与TNB-486格式相似,YZYBio公司的YBODY平台由一半与疾病靶点结合的IgG和一半与CD3结合的scFv组成。一些基于YBODY平台的TCE目前正在临床试验中,如M802(HER2/CD3)。
参考文献
[1]Baeuerle PA, Wesche H. T-cell-engaging antibodies for the treatment of solid tumors: challenges and opportunities. Curr Opin Oncol. 2022 Sep 1;34(5):552-558. doi: 10.1097/CCO.0000000000000869.
[2]Pillarisetti K, Powers G, Luistro L, et al.Teclistamab is an active T cell-redirecting bispecific antibody against B-cell maturation antigen for multiple myeloma. Blood Adv. 2020 Sep 22;4(18):4538-4549. doi: 10.1182/bloodadvances.2020002393.
[3]Smith, E., Olson, K., Haber, L. et al. A novel, native-format bispecific antibody triggering T-cell killing of B-cells is robustly active in mouse tumor models and cynomolgus monkeys. Sci Rep 5, 17943 (2016). https://doi.org/10.1038/srep17943.

澳门威斯人游戏平台[亚洲]全站最新版V11.37.7 Nanjing Detai Bioengineering Co.,Ltd. ©2024 All Rights Reserved
苏ICP备2021019379号-1 | 网站地图 | 用户协议 | 隐私政策